Từ điển hóa học
Tudienhoahoc.com là website tổng hợp trong lĩnh vực hóa học, trang web có các chức năng chuyên nghiệp như:
Từ điển phương trình hóa học với dữ liệu hơn 10.000 phương trình. Bao gồm thông tin của các chất tham gia và chất sản phẩm.
Từ điển chất hóa học với dữ liệu hơn 3.000 chất.
Ngoài ra còn có các bài viết chia sẻ về hóa học và đời sống, ứng dụng của hóa học vào cuộc sống hằng ngày.
Phản ứng hóa học nổi bậtinsert_link
Bài viết mới nhất
-
Mối quan hệ giữa các hợp chất vô cơ – Oxit, Axit, bazơ và muối
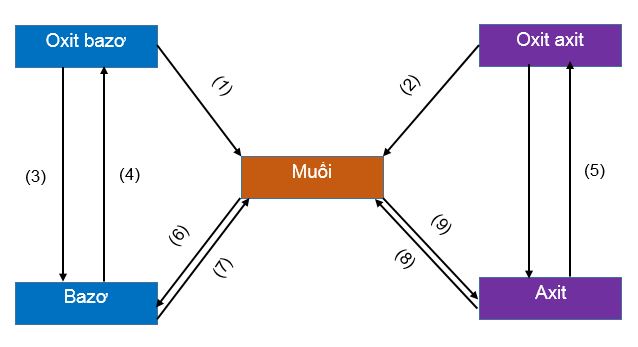
Chúng ta đã biết tính chất hóa học của oxit, axit, bazơ và muối. Vậy giữa chúng có mối liên hệ như thế nào? Điều kiện cho những chuyển đổi giữa các
-
ESTE – Khái niệm, danh pháp, tính chất hóa học, ứng dụng và điều chế

Este là gì? Este có những tính chất vật lý và hóa học như thế nào? Cách gọi tên este, ứng dụng và điều chế este như thế nào? Trong bài viết hôm nay, chúng ta
-
Tiểu sử Dmitri Mendeleev người phát minh ra bảng tuần hoàn

Dmitri Mendeleev (Men đê lê ép – sinh ngày 8 tháng 2 năm 1834, mất ngày 2 tháng 2 năm 1907) là một nhà khoa học người Nga nổi tiếng là người lập bảng tuần
-
Tính chất hóa học của muối – Phản ứng trao đổi trong dung dịch

Chúng ta đã biết đến nhiều loại muối. Vậy tính chất hóa học của muối là gì? Thế nào là phản ứng trảo đổi và điều kiện để xảy ra phản ứng trao
-
Dung dịch – Dung môi – Chất tan – Dung dịch bão hòa và chưa bão hòa

Trong cuộc sống hằng ngày, chúng ta hay nghe nhắc đến khái niệm dung dịch. Khi hòa tan muối hay đường vào nước, ta được các dung dịch muối, đường. Vậy dung
-
Axit cacbonic (H2CO3) và muối Cacbonat – Chu trình Cacbon trong tự nhiên

Axit cacbonic (H2CO3) và muối cacbonat có những tính chất và ứng dụng gì? Chúng ta sẽ cùng tìm hiểu hai hợp chất quan trọng của cacbon này nhé. Bên cạnh đó,
-
Silic – Silic đioxit (SiO2) – Công nghiệp sản xuất vật liệu silicat

Silic là một nguyên tố phi kim, phổ biến sau oxi trong vỏ Trái Đất. Vậy silic và những hợp chất của silic có những tính chất gì? Chúng ta sẽ cùng tìm hiểu
-
Những bài thơ vui về hóa học và tình yêu lãng mạn hấp dẫn

Thơ vui hóa học là chuyên mục trao đổi thơ ca về môn hóa học. Cùng nhau chia sẽ những bài thơ hay và câu chuyện ý nghĩa đến bạn đọc. Hôm nay, cùng thơ vui
-
Tính chất vật lý của kim loại – Tính dẻo, dẫn điện, dẫn nhiệt và ánh kim

Xung quanh chúng ta có rất nhiều đồ vật, máy móc làm bằng kim loại. Vậy kim loại có những tính chất vật lí gì. Những tính chất vật lí đó giúp kim loại có
-
Bom khói là gì? cách chế tạo và lắp ráp bom khói như thế nào?

Bom khói là gì? Cách chế tạo bom khói như thế nào? Chế tạo những quả bom khói kinh điển nhiều màu sắc sặc sỡ và an toàn có thể là một ý tưởng hay cho
-
Độ tan là gì? Những yếu tố ảnh hưởng đến độ tan của một chất
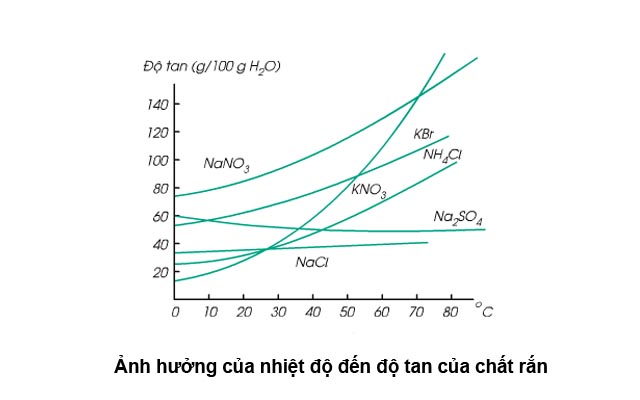
Trong cuộc sống, ta có thể bắt gặp những chất tan trong nước nhiều, những chất ít tan trong nước, hay có thể là những chất không tan trong nước. Vậy yếu
-
Một số oxit quan trọng: Canxi Oxit (CaO) và Lưu huỳnh đioxit (SO2)

Trong một số oxit quan trọng trong đời sống có thể kể đến 2 oxit: canxi oxit (CaO) và lưu huỳnh đioxit (SO2). Đây là 2 oxit quan trọng, ứng dụng nhiều trong đời