Như chúng ta đã biết, trong đời sống và sản xuất, các hợp kim của sắt là gang thép được sử dụng rất rộng rãi. Vậy bạn đã biết gang là gì, thép là gì chưa? Chúng gồm những thành phần nào và cách sản xuất chúng ra sao? Trong bài viết này, chúng ta sẽ cùng tìm hiểu về 2 hợp kim của sắt là gang và thép nhé!
I. Hợp kim của sắt
Hợp kim là chất rắn thu được sau khi làm nguội hỗn hợp nóng chảy của nhiều kim loại khác nhau hay của kim loại và phi kim.
Hợp kim của sắt có nhiều ứng dụng trong đời sống và sản xuất là gang và thép.
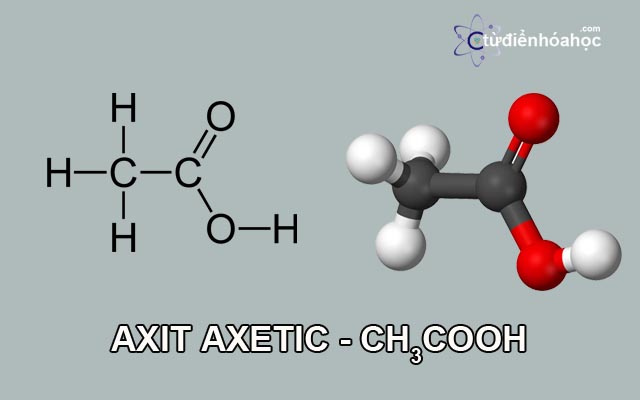
Hợp kim của sắt: gang, thép

hop-kim-cua-sat-gang-thep
1. Gang là gì?
Gang là hợp kim của sắt (Fe) với cacbon (chiếm 2 – 5%) và một số nguyên tố khác như: Mn, Si, S…
Gang cứng và giòn hơn sắt. Gang có 2 loại:
- Gang trắng: dùng để luyện thép
- Gang xám: dùng để đúc bệ máy, ống dẫn nước
2. Thép là gì?
Thép là hợp kim của sắt (Fe) với cacbon và một số nguyên tố khác. Trong đó, hàm lượng cacbon < 2%.
Thép có nhiều tính chất vật lý và hóa học ưu việt hơn sắt: cứng, đàn hồi và ít bị ăn mòn…
Thép được dùng để chế tạo các chi tiết máy, dụng cụ lao động, đồ gia dụng. Ngoài ra, thép còn ứng dụng rộng rãi trong ngành xây dựng chế tạo nhiều phương tiện giao thông như: xe lửa, ô tô, xe máy, xe đạp, tàu thuyền…
II. Sản xuất gang, thép như thế nào?
1. Sản xuất gang
a) Nguyên liệu
– Quặng sắt: quặng manhetit (chứa Fe3O4) và hematit (chứa Fe2O3)
– Than cốc, đá vôi, không khí giàu O2…
b) Nguyên tắc sản xuất gang
Nguyên tắc sản xuất gang là dùng CO khử oxit sắt ở t° cao trong lò luyện kim (lò cao).
c) Quá trình sản xuất gang trong lò cao
– Quặng sắt + than cốc + đá vôi được cho vào miệng lò cao và sắp thành từng lớp xen kẽ nhau. Không khi nóng được thổi từ dưới lên từ hai bên lò. Khi đó:
C + O2 (t°) → CO2
C+ CO2 (t°) → 2CO
– Khí CO sinh ra khử quặng sắt thành Fe: Một số oxit khác trong quặng sắt (như SiO, MnO…) cũng bị khử (thành Si, Mn…).
3CO + Fe2O3 (t°) → 2Fe + 3CO2
– Fe nóng chảy hòa tan một lượng nhỏ C và một số nguyên tố khác tạo thành gang lỏng. Gang lỏng chảy xuống nồi lò và được đưa ra ngoài qua cửa tháo gang.
– Đá vôi CaCO3 bị phân hủy thành CaO. CaO kết hợp với các oxit có trong quặng như SiO, MnO… tạo thành xỉ.
CaO + SiO2 (t°) → CaSiO3
– Xỉ nổi lên trên và được đưa ra ngoài ở cửa tháo xỉ
– Khí trong lò cao được thoát ra ngoài ở phía trên gần miệng lò.
Quang cảnh một nhà máy sản xuất gang thép

nha-may-san-xuat-gang-thep
2. Sản xuất thép
a) Nguyên liệu
– Nguyên liệu chính để sản xuất thép là gang, sắt phế liệu và oxi.
b) Nguyên tắc sản xuất thép
Nguyên tắc sản xuất gang là: oxi hóa một số kim loại và phi kim ra khỏi gang. Phần lớn các nguyên tố bị loại bỏ là Si, Mn, C…
c) Quy trình sản xuất thép
Quá trình sản xuất thép được thực hiện trong các lò luyện thép. Một trong những lò luyện thép quen thuộc là lò Bét-xơ-me.
– Khí O2 được thổi vào lò đựng gang nóng chảy ở t° cao. Khí O2 oxi hóa các kim loại và phi kim có trong gang như: Si, Mn, C, P, S…
Si + O2 (t°) → SiO2
C + O2 (t°) → CO2
III. Giải bài tập về những hợp kim của Sắt
Câu 1. Thế nào là hợp kim? Thế nào là gang và thép? Nêu thành phần, tính chất, ứng dụng của gang và thép.
Bài làm:
Các bạn xem lại trong phần lý thuyết ở trên nhé!
Câu 2. Hãy cho biết nguyên tắc sản xuất gang và viết các PTHH.
Bài làm: (xem chi tiết hơn trong phần lý thuyết)
– Nguyên tắc sản xuất gang: là dùng CO khử oxit sắt ở t° cao trong lò luyện kim (lò cao).
– Các PTHH trong quá trình sản xuất gang:
C + O2 (t°) → CO2
C+ CO2 (t°) → 2CO
3CO + Fe2O3 (t°) → 2Fe + 3CO2
CaO + SiO2 (t°) → CaSiO3
Câu 3. Hãy cho biết nguyên tắc luyện gang thành thép và viết các PTHH.
Bài làm: (xem chi tiết hơn trong phần lý thuyết)
– Nguyên tắc sản xuất gang là: oxi hóa một số kim loại và phi kim ra khỏi gang. Phần lớn các nguyên tố bị loại bỏ là Si, Mn, C…
– Các PTHH trong quá trình sản xuất thép:
Si + O2 (t°) → SiO2
2Mn + O2 (t°) → 2MnO
C + O2 (t°) → CO2
S + O2 (t°) → SO2
4P + 5O2 (t°) → 2P2O5
Câu 4. Những khí thải (CO2, SO2…) trong quá trình sản xuất gang, thép có ảnh hưởng như thế nào đến môi trường xung quanh? Dẫn ra một số phản ứng để giải thích. Thử nêu biện pháp để chống ô nhiễm môi trường ở khu dân cư gần cơ sở sản xuất gang thép.
Bài làm:
Khí CO2 và SO2 là nguyên nhân chính gây ra hiện tượng mưa axit ảnh hưởng đến các loài động thực vật, con người và các công trình xây dựng. Ngoài ra, khí CO2 còn là nguyên nhân gây ra hiện tượng hiệu ứng nhà kính, làm cho Trái Đất nóng lên.
Để hạn chế ô nhiễm môi trường do các khí này gây ra, chúng ta cần:
– Xử lý các khí thải trước khi thải ra môi trường bằng cách hấp phụ bằng nước vôi trong.
– Xây dựng các nhà máy luyện gang thép ở xa khu dân cư.
– Trồng nhiều cây xanh để lọc khí, làm giảm sự ảnh hưởng của các khí độc hại.
Câu 5. Hãy lập các PTHH theo sơ đồ sau đây:
a) O2 + 2Mn (t°) ‒‒‒> 2MnO
b) Fe2O3 + CO (t°) ‒‒‒> Fe + CO2
c) O2 + Si (t°) ‒‒‒> SiO2
d) O2 + S (t°) ‒‒‒> SO2
Cho biết phản ứng nào xảy ra trong quá trình luyện gang, phản ứng nào xảy ra trong quá trình luyện thép? Chất nào là chất oxi hoá, chất nào là chất khử ?
Bài làm:
a) O2 + 2Mn (t°) → 2MnO ⇒Chất khử: Mn ; chất oxi hóa: O2
b) Fe2O3 + 3CO (t°) → 2Fe + 3CO2⇒ Chất khử: CO ; chất oxi hóa: Fe2O3
c) O2 + Si (t°) → SiO2⇒Chất khử: Si ; chất oxi hóa: O2
d) O2 + S (t°) → SO2⇒ Chất khử: S ; chất oxi hóa: O2
Câu 6. Tính khối lượng quặng hematit chứa 60% Fe2O3 cần thiết để sản xuất được 1 tấn gang chứa 95% Fe. Biết hiệu suất của quá trình là 80%.
Bài làm:
– Khối lượng Fe có trong 1 tấn gang là:
mFe = 1 x 95/100 = 0,95 (tấn)
PTHH:
Fe2O3 + 3CO (t°) → 2Fe + 3CO2
– Khối lượng Fe2O3 cần dùng để sản xuất 0,95 tấn Fe là:
mFe2O3 = nFe2O3 x MFe2O3 = [(0,95 / 56) / 2] x 160 = 1,357 (tấn)
– Hiệu suất quá trình là 80% nên lượng Fe2O3 cần dùng là:
mFe2O3 = 1,357 x 100/80 = 1,696 (tấn)
– Do Fe2O3 chỉ chiếm 60% khối lượng trong quặng nên khối lượng quặng cần dùng là:
mquặng = 1,696 x 100/60 = 2,827 (tấn)