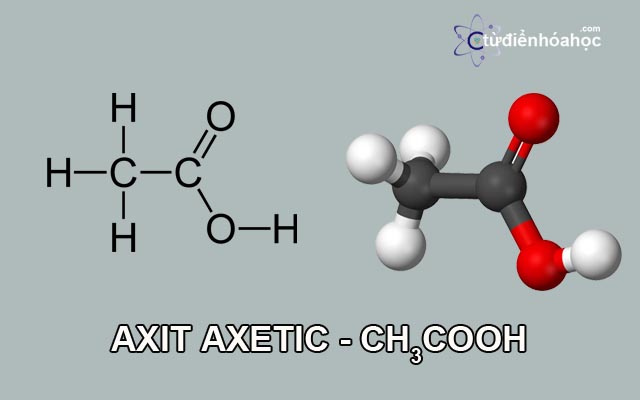
Từ xa xưa, con người đã biết sử dụng những vật dụng làm bằng sắt và những hợp kim của sắt. Ngày nay cũng vậy, sắt vẫn là kim loại được sử dụng nhiều nhất. Điều này là do sắt có những tính chất vật lý và hóa học đặc biệt. Vậy những tính chất vật lý và hóa học của sắt là gì, chúng ta sẽ cùng tìm hiểu trong bài viết hôm nay nhé!

tinh-chat-vat-ly-va-hoa-hoc-cua-sat
I. Tính chất vật lý và hóa học của Sắt
1. Tính chất vật lý của Sắt
Sắt (Fe) có nguyên tử khối bằng 56 đvC, có những tính chất vật lý sau:
– Sắt là kim loại nặng, có màu trắng xám và ánh kim
– Sắt có tính dẻo, dẫn nhiệt, dẫn điện tốt nhưng kém hơn Sắt
– Sắt có tính nhiễm từ
– Khối lượng riêng: 7,86 g/cm3
– Nhiệt độ nóng chảy: 1539 °C
2. Tính chất hóa học của Sắt
Sắt có đầy đủ tính chất hóa học đặc trưng của kim loại như:
2.1. Tác dụng với phi kim
a) Fe tác dụng với O2
Sắt tác dụng với oxi tạo thành oxit sắt từ, trong đó Fe có hóa trị (II) và (III).
3Fe + 2O2 (t°) → Fe3O4
Sắt tác dụng với oxi

sat-phan-ung-voi-oxi
b) Tác dụng với các phi kim khác
Sắt tác dụng với một số phi kim tạo thành muối.
2Fe + 3Cl2 (t°) → 2FeCl3
Fe + S (t°) → FeS
2Fe + 3Br2 (t°) → 2FeBr3
2.2. Tác dụng với dung dịch axit
Sắt tác dụng với một số dd axit (HCl, H2SO4 loãng …) tạo thành muối sắt (II) và giải phóng khí H2.
Fe + 2HCl → FeCl2 + H2 ↑
Fe + H2SO4 loãng → FeSO4 + H2 ↑
Fe không tác dụng với H2SO4 đặc, nguội và HNO3 đặc, nguội.
2.3. Tác dụng với dung dịch muối
Sắt tác dụng với dung dịch muối của những kim loại có hoạt động hóa học yếu hơn (như Cu, Ag, Pb…) tạo ra muối Sắt và kim loại mới.
Fe + CuSO4 → FeSO4 + Cu ↓
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag ↓
Fe + Pb(NO3)2 → Fe(NO3)2 + Pb ↓
II. Ứng dụng của sắt
Sắt và hợp kim của sắt có rất nhiều ứng dụng trong đời sống và sản xuất.
Ứng dụng của sắt trong đời sống và sản xuất
– Vật liệu cho ngành xây dựng
– Ứng dụng trong công nghiệp sản xuất ô tô và tàu thủy
– Làm đồ gia dụng và nội thất…

ung-dung-cua-sat
Giải bài tập tính chất vật lý hóa học và ứng dụng của sắt
Câu 1. Sắt có những tính chất hoá học nào? Viết các PTHH minh hoạ.
Bài làm:
Những tính chất hóa học của sắt:
a) Tác dụng với phi kim
– Fe tác dụng với O2 → oxit sắt từ (hỗn hợp của FeO và Fe2O3):
3Fe + 2O2 (t°) → Fe3O4
– Fe tác dụng với các phi kim khác như Cl2, Br2, S… tạo thành muối.
2Fe + 3Cl2 (t°) → 2FeCl3
Fe + S (t°) → FeS
2Fe + 3Br2 (t°) → 2FeBr3
b) Tác dụng với dung dịch axit
Sắt tác dụng với một số dd axit (HCl, H2SO4 loãng …) tạo thành muối sắt (II) và giải phóng khí H2.
Fe + 2HCl → FeCl2 + H2 ↑
Fe + 2HNO3 loãng → Fe(NO3)2 + H2 ↑
Fe + H2SO4 loãng → FeSO4 + H2 ↑
Fe không tác dụng với H2SO4 đặc, nguội và HNO3 đặc, nguội.
c) Tác dụng với dung dịch muối
Sắt tác dụng với dung dịch muối của những kim loại có hoạt động hóa học yếu hơn (như Cu, Ag, Pb…) tạo ra muối Sắt và kim loại mới.
Fe + CuCl2 → FeCl2 + Cu ↓
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag ↓
Câu 2. Từ Fe và các hoá chất cần thiết, hãy viết các PTHH để thu được các oxit sắt riêng biệt sau đây: Fe3O4, Fe2O3 và ghi rõ điều kiện phản ứng, nếu có.
Bài làm:
a) Điều chế Fe3O4:
3Fe + 2O2 (t°) → Fe3O4
b) Điều chế Fe2O3:
2Fe + 3Cl2 (t°) → 2FeCl3
FeCl3 + 3NaOH → Fe(OH)3 ↓ + 3NaCl
2Fe(OH)3 (t°) → Fe2O3 + 3H2O
Câu 3. Có bột kim loại Fe lẫn tạp chất Al. Hãy nêu phương pháp làm sạch sắt.
Bài làm:
– Cách 1: Dùng một miếng vải mỏng bọc lấy thanh nam châm rồi lăn nhẹ qua hỗn hợp bột Fe có lẫn Al. Do Fe có tính nhiễm từ nên bị nam châm hút. Ta làm nhiều lần cho đến khi Fe được tác hết ra khỏi hỗn hợp trên.
– Cách 2: Cho hỗn hợp trên vào dung dịch NaOH dư. Al bị hòa tan hoàn toàn trong dung dịch NaOH. Lọc lấy chất rắn còn lại, rửa sạch và sấy khô ta được Fe.
2Al + 2NaOH dư + 2H2O → 2NaAlO2 + 3H2 ↑
Fe + NaOH → Không phản ứng
Câu 4. Fe tác dụng được với chất nào sau đây?
a) dd muối Cu(NO3)2
b) H2SO4 đặc, nguội
c) Khí Cl2
d) dd ZnSO4
Viết các PTHH và ghi điều kiện, nếu có.
Bài làm:
Fe tác dụng được với: dung dịch muối Cu(NO3)2 và khí Cl2. Fe không tác dụng được với H2SO4 đặc, nguội và dung dịch ZnSO4.
PTHH:
Fe + Cu(NO3)2 →Fe(NO3)2 + Cu ↓
2Fe + 3Cl2 (t°) → 2FeCl3
Câu 5. Ngâm bột Fe dư trong 10 ml dd đồng sunfat CuSO4 1M. Sau khi phản ứng kết thúc, lọc được chất rắn A và dung dịch B.
a) Cho A tác dụng với dd HCl dư. Tính khối iượng chất rắn còn lại sau phản ứng.
b) Tính thể tích dd NaOH 1M vừa đủ để kết tủa hoàn toàn dd B.
Bài làm:
PTHH:
Fe + CuSO4 → FeSO4 + Cu ↓
Do bột Fe dư nên chất rắn A gồm Fe dư và Cu. Dung dịch B là FeSO4.
Ta có:
nCuSO4 = CM x V = 1 x 0,01 = 0,01 (mol)
⇒ nCu = nFeSO4 = nCuSO4 = 0,01 (mol)
a) Cho A tác dụng với HCl dư:
Fe dư + 2HCl → FeCl2 + H2 ↑
Cu + HCl → Không phản ứng
⇒ Chất rắn còn lại sau phản ứng với dd HCl là Cu và có khối lượng là:
mCu = nCu x MCu = 0,01 x 64 = 0,64 (g)
b) Phản ứng làm kết tủa dung dịch B:
2NaOH + FeSO4 → Fe(OH)2 ↓ + Na2SO4
Theo PT, ta có: nNaOH = 2 x nFeSO4 = 2 x 0,01 = 0,02 (mol)
⇒ Thể tích dung dịch NaOH 1M cần dùng là:
VNaOH = nNaOH/CM NaOH = 0,02 / 1 = 0,02 lít = 20 ml.