Nước cứng (hard water) đang là nỗi ám ảnh với nhiều doanh nghiệp bởi chúng gây ra những thiệt hại không hề nhỏ. Ngoài ra, nước cứng gây không ít khó khăn cho cuộc sống chúng ta. Vậy nước cứng là gì? Phân loại, đơn vị đo, nguyên nhân hình thành và xử lý như thế nào để làm mềm nước cứng?
Nước cứng là gì và nước mềm là gì ? Đây là 2 khái niệm quen thuộc của hóa học đời sống nhưng chúng ta chưa hiểu biết đầy đủ về chúng? Bài viết dưới đây, Từ Điển Hóa Học chia sẻ với các bạn có được cái nhìn toàn diện hơn về nước mềm và nước cứng.
Bài viết liên quan:
- Nước đá khô là gì? Giải thích tất tần tật những điều bạn nên biết
- Sự điện li của nước, Cách tính độ pH, Chất chỉ thị axit-bazơ là gì?
1. Nước cứng là gì?
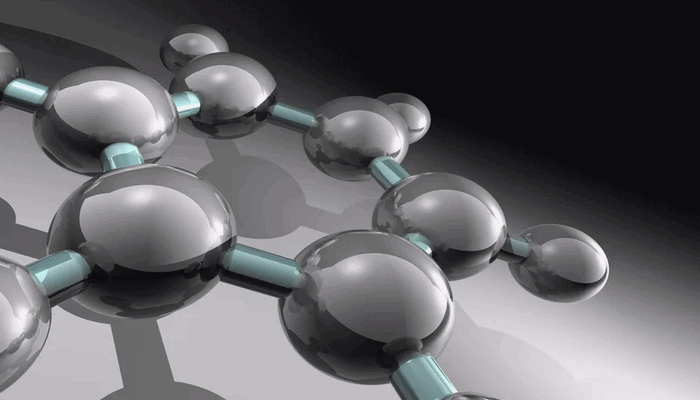
– Nước cứng (hard water) là loại nước chứa nhiều ion Ca2+và Mg2+. Các khoáng chất có trong nước cứng bao gồm các hợp chất của ion kim loại canxi, magie dưới dạng cacbonat, canxi cacbonat và magie cacbonat hoặc các hợp chất kim loại caxi, magie với sunfat, bicacbonat, clorua.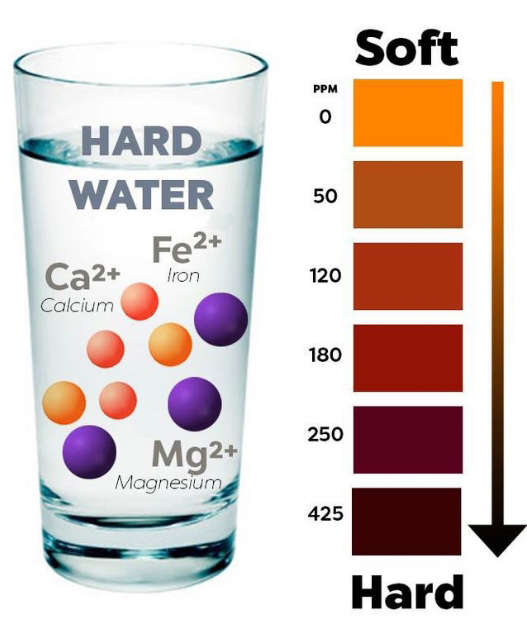
Hình ảnh tổng quan về nước cứng – Nước cứng là gì ?
– Nước mềm là nước không chứa hoặc chứa một lượng không đáng kể các ion Ca2+và Mg2+.
2. Có mấy loại nước cứng
– Nước cứng tạm thời: chứa mối hidro cacbonat như Ca(HCO3)2, Mg(HCO3)2 ít hơn và có cả Fe(HCO3)2. Vì các muối này bị phân hủy do đun sôi, mất đi tính cứng. Lúc đó, các muối hidrocacbonat đã tan biến thành cacbonat không tan lắng xuống thanh cặn
Ca(HCO3)2 → CaCO3 + H2O + CO2
Mg(HCO3)2 → MgCO3 + H2O + CO2
– Nước cứng vĩnh cửu: chứa muối của ion Magie, canxi với các gốc anion của axit mạnh như (Cl)– và (SO4)2- như CaSO4, MgSO4, MgCl2,…
– Nước cứng toàn phần: chứa cả muối của ion Ca2+, Mg2+ và (Cl)–, (SO4)2- (gồm nước cứng tạm thời và nước cứng vĩnh cửu
– Độ cứng của nước bằng tổng của độ cứng tạm thời và động cứng vĩnh cữu.
3. Độ cứng của nước là gì?
Độ cứng của nước thông thường thì được chia thành 2 loại đó là:
– Độ cứng tạm thời hay còn được gọi là độ cứng carbonat: được gọi là độ cứng tạm thời bởi vì nó còn được giảm bởi những phương pháp khá đơn giản. Về cấu tạo của độ cứng tạm thời thì nó còn được cấu tạo bởi những yếu tố như Ca, Mg, carbonat và bicarbonat.
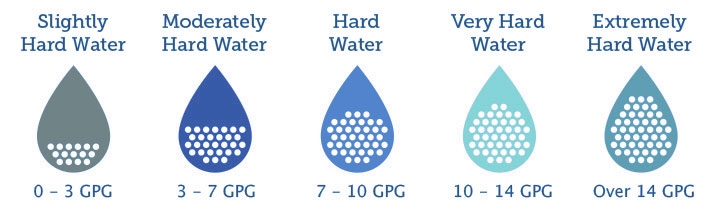 Hình ảnh độ cứng của nước cứng
Hình ảnh độ cứng của nước cứng
– Độ cứng vĩnh viễn: Tạo bởi các muối khác của Ca và Mg như sulphat, clorua… chỉ có thể thay đổi bằng các phương pháp phức tạp và đắt tiền.
– Không những thế nước có một độ cứng tạm thời lớn hơn 100 ppm được coi là nước cứng, dưới mức đó được coi là nước mềm. Và thông thường người ta chỉ quan tâm đến độ cứng tạm thời của nước vì nó có ảnh hưởng nhiều hơn là độ cứng vĩnh viễn.
4. Đơn vị đo độ cứng của nước
– Tổng độ cứng của nước là tổng nồng độ của các ion Ca2+và Mg2+
– Có nhiều đơn vị đo độ cứng khác nhau, nhưng chủ yếu người ta dùng 3 đơn vị đo. Vào những năm 1960, nhà khoa học Chris Gilby đã khám phá ra rằng nước cứng có thể được phân loại bởi các ion tìm thấy trong nước.
 Đơn vị đo nước cứng là gì ?
Đơn vị đo nước cứng là gì ?
Độ cứng có đơn vị Deutsche Härte (°dH của nước Đức). Ngoài ra, chưa có sự thống nhất đơn vi một số nước khác như đơn vị 0f (của nước Pháp), 0e (của nước Anh). Ở Việt Nam dùng đơn vị mg đương lượng/lít và ppm. Để đơn giản, khi đo độ cứng người ta thường quy về 1 loại muối là CaCO3.
 Quy đổi một số đơn vị đo độ cứng
Quy đổi một số đơn vị đo độ cứng
– Đơn vị đo tại Việt nam là mg đương lượng/lít: Độ cứng của nước có thể tính bằng số mili đương lượng game (mdlg/l) của kim loại hóa trị hai có trong 1 lít nước.
- Nước rất mềm: <1.5 mdlg/l
- Nước mềm: 1.5 – 4 mdlg/l
- Nước trung bình: 4 – 8 mdlg/l
- Nước cứng: 8 – 12 mdlg/l
- Nước rất cứng: >12 mdlg/l
Để biết được độ cứng của nước là bao nhiêu thì ta có thể sử dụng các máy đo độ cứng chuyên dụng để kiểm tra chúng.
5. Nguồn gốc của nước cứng
– Cacbon dioxide chiếm 0.3% không khí trái đất và dễ dàng hấp thu bởi nước để tạo thành axit cacbonic. Vì thế, mưa có tinha axit và có xu hướng hòa tan khoáng chất và đá. Khi có nước mưa, nước di chuyển qua lớp đất và đá, qua đó nó hòa tan một lượng khoáng chứa kim ion Ca2+ , Mg2+ hòa tan thành dung dịch.
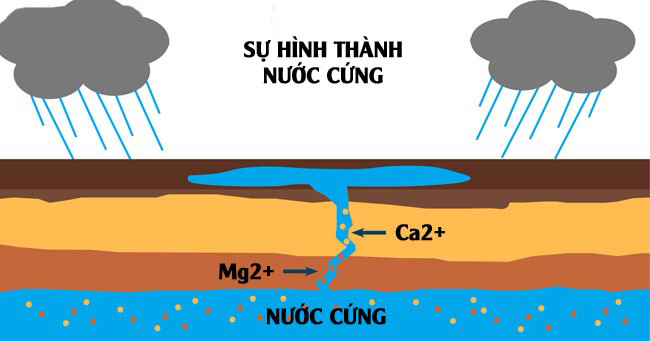 Hình ảnh quá trình hình thành của nước cứng
Hình ảnh quá trình hình thành của nước cứng
– Từ đầu nguồn, nước chảy thành dòng qua những địa hình khác nhau, hòa tan các nguyên tố vi lượng trong đất đá bao gồm cả canxi và magie. Quá trình hòa tan này làm tăng lượng ion kim loại gây ra tình trạng nước cứng.
– Nước có độ cứng cao thường là từ các nguồn nước ngầm. Nước ngầm đi qua các lớp đất đá, các lớp đá vôi, trầm tích từ đó hòa tan các ion Ca2+, Mg2+… trong các lớp trầm tích, đá vôi… làm tăng độ cứng trong nước. Nước ở ao hồ, sông suối cũng có thể bị tăng độ cứng do nguyên nhân này.
6. Ảnh hưởng của nước cứng
6.1. Ảnh hưởng của nước cứng đến đời sống
Nước cứng ảnh hưởng không nhỏ đến đời sống sinh hoạt hàng ngày và sức khỏe con người.
– Nước nhiễm canxi không thể dùng để pha chế thuốc vì có thể gây kết tủa làm thay đổi thành phần của thuốc.
– Nước cứng làm mất mùi vị ngon ngọt tự nhiên của nước nên ít dùng để pha đồ uống như giảm vị trà, thay đổi màu sắc và mùi vị của sữa, cà phê khiến cho các loại đồ uống có màu đậm, vị ngang hoặc chát, ít thơm, ít ngọt.
– Nước cứng cũng được khuyến cáo không nên sử dụng để sắc hay chế thuốc bắc, nam bởi các ion trong nước tác dụng với những thành phần thuốc có thể gây ra nhiều tác dụng phụ nguy hiểm.
 Hình ảnh tác hại của nước cứng đối với đời sống
Hình ảnh tác hại của nước cứng đối với đời sống
– Tạo các kết tủa với xà phòng ((C15H31COO)2Na, (C15H31COO)2Mg,…) Làm cho xà phòng ít tan khi giặc, quần áo nhanh hỏng do hình thành các kết tủa khó tan bám trên quần áo.
– Các đồ dùng nhà bếp dùng để đun nấu như nồi hơi, hoặc nước bình nóng lạnh, dễ bị bám cặn, nhanh làm hỏng sản phẩm.
– Dùng nước cứng tắm gội hàng ngày sẽ gây khô da, khô tóc
6.2. Ảnh hưởng của nước cứng đến với sức khỏe
Nước cứng tạm thời khi đi vào cơ thể thì muối bicarbonat bị phân hủy tạo thành muối cacbonat kết tủa (Ca(HCO3)2 → CaCO3). CaCO3 không thấm qua được thành ruột và động mạch nên tích tụ trong các cơ quan của cơ thể, lâu ngày sẽ tạo thành sỏi hoặc làm tắc những đường động mạch, tĩnh mạch gây nguy hiểm đến sức khỏe.
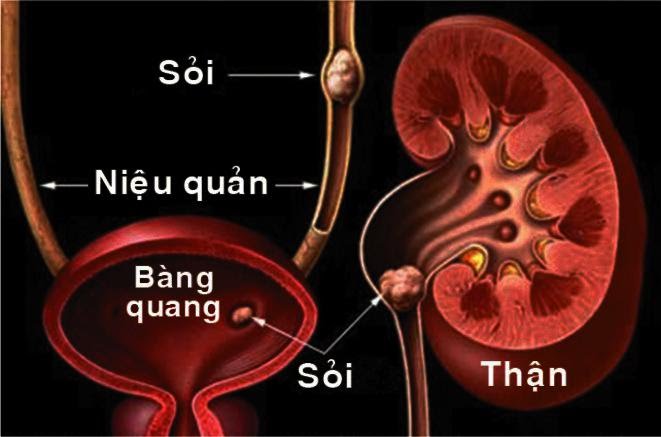
Uống nước cứng lâu ngày tăng nguy cơ sỏi thận, sỏi tiết niệu
6.3. Ảnh hưởng của nước cứng đến công nghiệp
– Lớp CaCO3 hình thành do nước cứng có thể tạo thành 1 lớp cách nhiệt dưới đáy nồi hơi, làm giảm khả năng dẫn và truyền nhiệt, làm tiêu hao điện năng gây lãng phí.
 Hình ảnh ảnh hưởng của nước cứng đối với đường ống trong công nghiệp
Hình ảnh ảnh hưởng của nước cứng đối với đường ống trong công nghiệp
– Nước cứng làm cho các thiết bị công nghiệp như nồi hơi, thiết bị lạnh… dẫn đến tình trạng bám cặn trên bề mặt thiết bị đun nấu, làm giảm hệ số lưu thông lưu lượng trên đường ống, dần dần có thể gây áp lực lớn gây nổ nổi hơi.
– Nước cứng gây nhiều phiền toái trong cuộc sống, vậy cách khắc phục nước cứng như thế nào hiệu quả?
7. Nhận biết nước cứng như thế nào
– Đóng cặn dưới đáy bình đun nước
– Xà phòng bị giảm bọt và mất khả năng làm sạch.
 Hình ảnh xà phòng giảm bọt do tác dụng của nước cứng
Hình ảnh xà phòng giảm bọt do tác dụng của nước cứng
– Bình nóng lạnh đun lâu nóng
– Vòi sen, vòi nước bị tắt nghẽn
 Hình ảnh nước cứng làm ngẹt vòi nước
Hình ảnh nước cứng làm ngẹt vòi nước
– Đường ống dẫn nước bị đóng cặn bã, tốc độ dòng chảy giảm xuống bất thường
– Quần áo khi giặc bị ố màu, chuyển sang màu ám vàng
– Khi pha trà thì mùi hương của nước trà sau khi pha giảm đi rất nhiều
8. Phương pháp làm mềm nước cứng
8.1. Nguyên tắc làm mềm nước cứng
– Làm giảm nồng độ ion Ca2+ và Mg2+ trong nước cứng
8.2. Phương pháp kết tủa
+ Xử lý nước cứng tạm thời:
Dùng một lượng Ca(OH)2 để kết tủa ion Ca2+ Ca(HCO3)2 và ion Mg2+ (Mg(HCO3)2), muối cacbonat của Ca, Mg kết tủa lắng xuống. Sau đó tiến hành lọc kết tủa.
Ca(HCO3)2 + Ca(OH)2 → 2CaCO3 + 2H2O
Mg(HCO3)2 + Ca(OH)2 → CaCO3 + MgCO3 + 2H2O
8.3. Phương pháp nhiệt
Cơ sở lý thuyết của phương pháp này là dùng nhiệt (đun sôi) để bốc hơi khí cacbonic hòa tan trong nước. Trạng thái cân bằng của các hợp chất cacbonic sẽ chuyển dịch theo phương trình phản ứng sau:
2HCO3 – → CO32- + H2O + CO2
Ca2+ + CO32- → CaCO3 ↓
Nên Ca(HCO3)2 → CaCO3 ↓ + CO2 + H2O
Tuy nhiên, khi đun nóng nước chỉ khử được hết khí CO2 và giảm độ cứng cacbonat của nước, còn lượng CaCO3 hòa tan vẫn còn tồn tại trong nước.
+ Xử lý nước cứng vĩnh cửu: dùng Na2CO3 hoặc Na3PO4 để kết tủa Các muối chứa ion SO42-, Cl–.. của kim loại kiềm. Sau đó tiến hành lọc kết tủa.
CaSO4 + Na2CO3 → CaCO3 + Na2SO4
MgCl2 + Na3PO4 → Mg2(PO4)3 + NaCl
8.4. Phương pháp trao đổi ion
Những hợp chất có khả năng trao đổi cation được gọi là cationit. Những hợp chất có khả năng trao đổi anion được gọi là anionit. Phương pháp trao đổi ion được ứng dụng dựa trên khả năng có thể trao đổi ion của của một số hợp chất cao phân tử gọi là ionit.
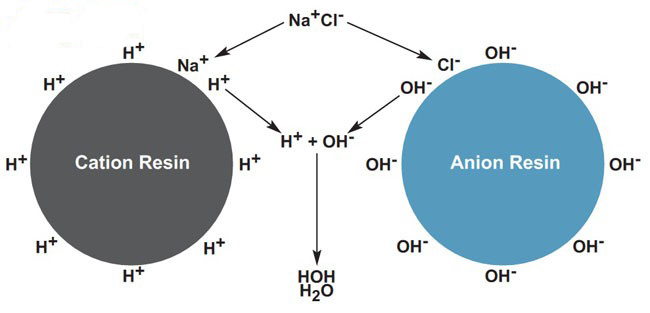 Làm mềm nước cứng bằng phương pháp trao đổi ion
Làm mềm nước cứng bằng phương pháp trao đổi ion
Nguyên lý trao đổi ion là quá trình trao đổi thay thế giữa các ion dương hay âm cố định trên các gốc axit hay bazo của vật liệu hạt trao đổi ion cùng dấu có trong dung dịch lỏng khi có sự tiếp xúc. Sự khác biệt của công nghệ làm mềm nước này thể hiện ở cấu tạo và quy trình công nghệ sản xuất vật liệu trao đổi ion.
Thông thường các ion dùng để trao đổi thường là các ion lành tính như Na+ hoặc H+. Khi cho nguồn nước dẫn qua các vật liệu lọc thì các ion Ca2+ và Mg2+ sẽ bị giữ lại trên bề mặt vật liệu. sử dụng dài ngắn khác nhau.
Người ta thường dùng Zeolit là một loại cationit (natrisilicat) thiên nhiên hay nhân tạo để trao đổi ion Na+ với các ion Ca2+ & Mg2+ của nước cứng:
Nước cứng (Ca2+ & Mg2+ ) + Zeolit (Na+) →
Nước mềm (Na+) + Zeolit (Ca²+ Mg²+) →
Minh họa bằng phương trình:
Na2Al2Si2O8.xH2O + Ca(HCO3)2 → CaAl2Si2O8.xH2O + 2NaHCO3
Sau đó tái sinh Zeolit bằng NaCl:
CaAl2Si2O8.xH2O + 2NaCl → Na2Al2Si2O8.xH2O + CaCl2
Ngày nay, phương pháp trao đổi ion được sử dụng phổ biến và rất hiệu quả trong xử lí nước cứng. Bằng cách sử dụng các vật liệu Polyme chứa các ion trao đổi. Các ion này (Chủ yếu là cation Na+) có khả năng trao đổi và thay thế các ion Ca²+ & Mg²+ trong nước cứng. Từ đó làm giảm nồng độ của các ion này.
8.5. Quy trình xử lí nước cứng bằng phương pháp trao đổi ion
Bước 1: Nước cứng chảy qua, các vật liệu lọc trong hệ thống lọc nước: Các vật liệu lọc này hoạt động như một nam châm, thu hút toàn bộ các ion Ca2+ và Mg2+ (tác nhân gây cứng nước) trao đổi với các ion Na+ hoặc H+ có sẵn trong vật liệu
Bước 2: Vật liệu lọc bị bão hòa: Khi vật liệu lọc bị bão hòa với các ion khoáng chất thì nó cần được xả và nạp lại. Quá trình này được gọi là quá trình tái tạo và được kiểm soát bởi 1 van điều khiển trên nắp của bình. Van điều khiển này là bộ não của toàn hệ thống.
Bước 3: Tái tạo: Trong quá trình này, một thùng chứa nước muối sẽ bơm nước muối sang cột xử lý, rửa sạch vật liệu lọc đang trong trạng thái bão hòa các chất canxi và magiê.
Bước 4: Đào thải: Các ion Ca2+ và Mg2+ được tẩy sạch trên vật liệu và thoát ra ngoài cống rãnh. Vật liệu lọc được tái sinh lại tiếp tục cho quá trình xử lý mới.
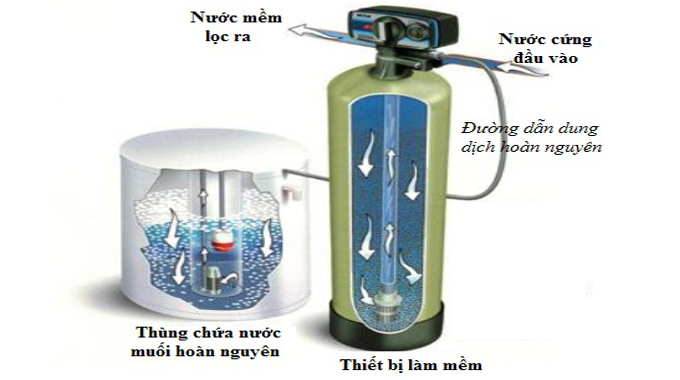 Hình ảnh tổng thể quy trình làm mềm nước cứng
Hình ảnh tổng thể quy trình làm mềm nước cứng
Phương pháp làm mềm nước cứng toàn phần cho nước cứng đi qua 2 cột trao đổi ion. Một cột đựng nhựa cationit và một cột đựng nhựa anionit. Nhựa cationit là hợp chất cao phân tử hữu cơ chứa nhóm axit, có công thức chung là RCOOH (R là gốc hữu cơ phức tạp). Qua cột này, các cation trong nước bị giữ lại và trong nước sinh ra axit.
2RCOOH + CaSO4 → Ca(RCOO)2 + H2SO4
RCOOH + NaCl → RCOONa + HCl
Nhựa anionit là những hợp chất cao phân tử hữu cơ chứa nhóm bazo có công thức chung RNH3OH. Qua cột này axit được giữ lại.
2RNH3OH + H2SO4 → (RNH3)2SO4 + 2H2O
RNH3OH + HCl → RNH3Cl + H2O
Tái sinh nhựa tro đổi ion: đưa dung dịch axit qua cột đựng nhựa cationit và đưa dung dịch kiềm qua cột anionit
2NaRCOO + H2SO4 → 2RCOOH + Na2SO4
(RNH3)Cl + NaOH → RNH3OH + NaCl
Nước cứng gây ảnh hưởng tiêu cực tới sức khỏe và cuộc sống sinh hoạt của các hộ gia đình. Tuy nhiên, sự phát triển của hóa học thì kiến thức về nước cứng cũng được khám phá như phân loại, đơn vị đo, nguồn gốc, ảnh hưởng và cách làm mềm đầy đủ nhất. Bên cạnh đó, bài viết nước cứng là gì chia sẽ phương pháp làm mềm nước cứng hiện đại nhất và được áp dụng thực tế trong đời sống và công nghiệp hiện nay.