Để bảo vệ vỏ tàu biển người ta dùng phương pháp chống ăn mòn kim loại. Các thiết bị, máy móc, phương tiện tàu biển, các kết cấu công trình, các vật liệu kim loại…. sau một thời gian làm việc, sẽ bị gỉ sét và dần dần bị ăn mòn trong điều kiện môi trường sử dụng. Các hiện tượng trên là do quá trình ăn mòn kim loại gây nên.
Nhằm giúp cho học sinh biết cách vận dụng kiến thức để giải thích hiện tượng trong cuộc sống. Hôm nay cùng Từ Điển Hóa Học giải thích quá trình ăn mòn vỏ mạn tàu thủy. Đồng thời giải thích vì sao các cơ sở đóng tàu thường gắn một miếng kim loại Kẽm trên tàu.
1. Cơ sở lý thuyết ăn mòn kim loại tàu biển
1.1. Khái niệm ăn mòn kim loại
Là sự phá hủy kim loại hoặc hợp kim của chúng do tác dụng hoá học hoặc tác dụng điện hoá giữa kim loại và môi trường bên ngoài.
 Hình ảnh ăn mòn kim loại tàu biển
Hình ảnh ăn mòn kim loại tàu biển
1.2. Phân loại ăn mòn kim loại
1.2.1. Ăn mòn hóa học
Là quá trình oxi hóa khử, trong đó các electron của kim loại được chuyển trực tiếp đến các chất trong môi trường.

Ví dụ: Các vật dụng bằng sắt để ngoài không khí sẽ bị rgỉ sét
3Fe + 4H2O → Fe3O4 + 4H2
2Fe + 3Cl2 → 2FeCl3
3Fe + 2O2 → Fe3O4
Ăn mòn hóa học thường xảy ra ở những bộ phận của thiết bị lò đốt hoặc những thiết bị thường xuyên phải tiếp xúc với hơi nước và khí oxi…
1.2.2. Ăn mòn điện hóa
Là quá trình oxi hóa khử, trong đó kim loại bị ăn mòn do tác dụng của dung dịch chất điện li và tạo nên dòng electron chuyển dời từ cực âm đến cực dương.
Thí dụ: phần vỏ tàu biển chìm trong nước, ống dẫn đặt trong lòng đất, kim loại tiếp xúc với không khí ẩm… Do vậy, ăn mòn điện hóa là loại ăn mòn kim loại phổ biến và nghiêm trọng nhất
– Sự ăn mòn điện hóa một vật bằng gang (hợp kim Fe – C)(hoặc thép) trong môi trường không khí ẩm có hòa tan khí CO2, SO2, O2… sẽ tạo ra một lớp dung dịch điện li phủ bên ngoài kim loại.
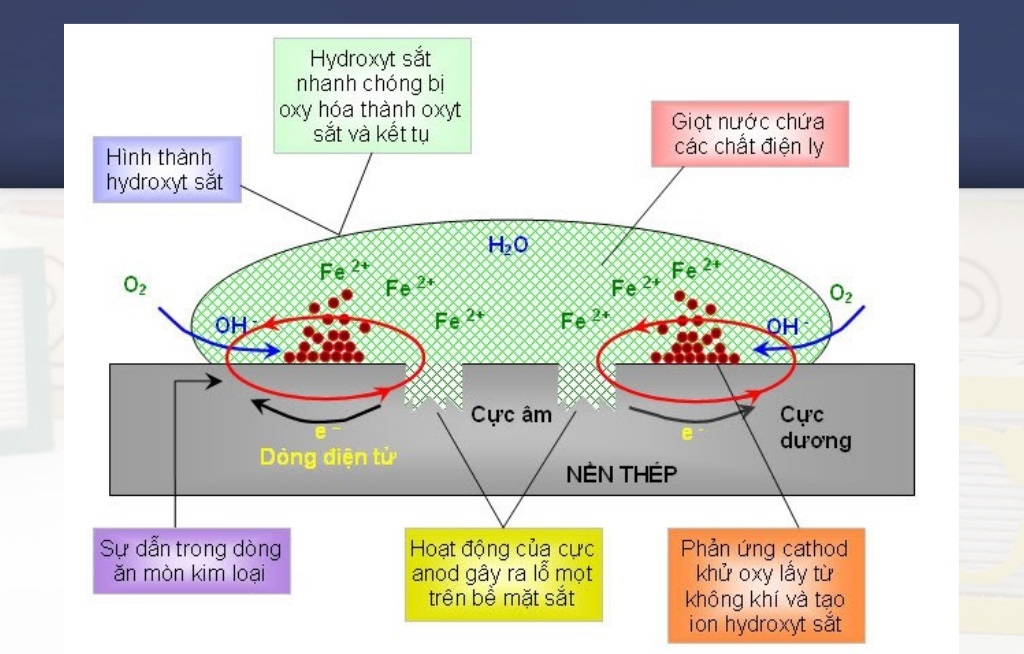 Hình ảnh minh họa quá trình ăn mòn thép
Hình ảnh minh họa quá trình ăn mòn thép
– Tinh thế Fe (cực âm), tinh thể C là cực dương.
Ở cực dương: xảy ra phản ứng khử:
2H+ + 2e → H2 ; O2 + 2H2O + 4e → 4OH–
Ở cực âm: xảy ra phản ứng oxi hóa:
Fe → Fe2+ + 2e
Những Fe2+ tan vào dung dịch chứa oxi → Fe3+ và cuối cùng tạo gỉ sắt có thành phần Fe2O3.nH2O
– Điều kiện để xảy ra ăn mòn điện hóa: phải thỏa mãn đồng thời 3 điều sau:
- Các điện cực phải khác nhau về bản chất
- Các định cực phải tiếp xúc trực tiếp hoặc gián tiếp với nhau qua dây dẫn
- Các điện cực cùng tiếp xúc với dung dịch chất điện li
– Ăn mòn điện hóa thường xảy ra khi cặp kim loại (hoặc hợp kim) để ngoài không khí ẩm, hoặc nhúng trong dung dịch axit, dung dịch muối, trong nước không nguyên chất…
2. Các biện pháp chống ăn mòn kim loại
2.1. Phương pháp bảo vệ bề mặt
– Phủ lên bề mặt kim loại một lớp sơn, dầu mỡ, chất dẻo…
– Lau chùi, để nơi khô ráo thoáng

Kỹ sư đang sơn lớp phủ để bảo vệ loại để chống ăn mòn kim loại tàu biển
2.2. Phương pháp điện hóa
– Dùng một kim loại là “vật hi sinh” để bảo vệ vật liệu kim loại:
- Kim loại – kim loại (Fe – Cu) kim loại mạnh bị ăn mòn (anot bị oxi hóa) kim loại yếu được bảo vệ
- Kim loại – phi kim (Fe – C thép)
- Kim loại đẩy kim loại ra khỏi muối (Fe tác dụng dung dịch CuSO4).
- Kim loại + dd axit và muối của kim loại đứng sau
3. Ăn mòn kim loại tàu biển
Sự ăn mòn kim loại tàu biển diễn ra rất nhanh và mạnh trong nước biển. Điều kiện môi trường này xảy ra sự phá hủy kim loại do ăn mòn điện hóa. Sự ăn mòn các con tàu kim loai khổng lồ, hiện đại đã đặt ra nhiều nghiên cứu để khác phục hiện tượng tai hại này. Có một biện pháp mà nhiều bạn đọc thắc mắc là vì sao, gắn tấm kim loại kẽm vào tàu biển có thể chống ăn mòn kim loại tàu biển.
Vì sao ở các cơ sở đóng tàu thường gắn một miếng kim loại Kẽm Zn ở phía sau đuôi tàu để Chống ăn mòn kim loại?
Sự ăn mòn kim loại đặc biệt là ăn mòn điện hóa hàng năm gây tổn thất thật nghiêm trọng cho nền kinh tế quốc dân. Con người luôn cố gắng tìm ra những phương pháp chống ăn mòn kim loại. Phương pháp điện hóa để chống ăn mòn kim loại. Dùng kim loại Kẽm để bảo vệ vỏ tàu biển như trên rất hiệu quả và được ứng dụng rất rộng rãi.
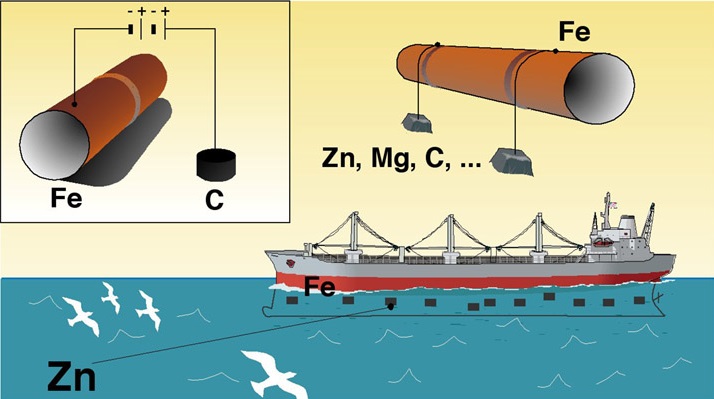 Chống ăn mòn kim loại – dùng kẽm để bảo vệ vỏ tàu biển
Chống ăn mòn kim loại – dùng kẽm để bảo vệ vỏ tàu biển
Thân tàu biển được chế tạo bằng gang thép. Gang thép là hợp kim của sắt, cacbon và một số nguyên tố khác. Đi lại trên biển, thân tàu tiếp xúc thường xuyên với nước biển là dung dịch chất điện li nên sắt bị ăn mòn, gây hư hỏng.
Để bảo vệ thân tàu người thường áp dụng biện pháp sơn nhằm không cho gang thép của thân tàu tiếp xúc trực tiếp với nước biển. Nhưng ở phía đuôi tàu, do tác động của chân vịt, nước bị khuấy động mãnh liệt nên biện pháp sơn là chưa đủ. Do đó mà phải gắn tấm kẽm vào đuôi tàu.
Vì khi gắn miếng Zn lên vỏ tàu bằng thép sẽ hình thành một pin điện, phần vỏ tàu bằng thép là cực dương, các lá Zn là cực âm và bị ăn mòn theo cơ chế:
– Ở anot (cực âm): Zn → Zn2+ + 2e
– Ở catot (cực dương): 2H2O + O2 + 4e → 4OH–
Khi đó sẽ xảy ra quá trình ăn mòn điện hóa. Kẽm là kim loại hoạt động hơn sắt nên bị ăn mòn, còn sắt thì không bị mất mát gì. Sau một thời gian miếng kẽm bị ăn mòn thì sẽ được thay thế theo định kỳ. Việc này vừa đở tốn kém hơn nhiều so với sửa chữa thân tàu.
Hiện tượng ăn mòn kim loại – ăn mòn kim loại tàu biển đang xảy ra phổ biến trong đời sống. Tuy nhiên, hiện tượng này đã được nhiều nhà khoa học nghiên cứu và tìm ra cách chống lại sự ăn mòn kim loại như sơn chống ăn mòn, các kim loại hy sinh bảo vệ kim loại, hay nghiên cứu các vật liệu chống ăn mòn,…