Bảng tính tan đầy đủ và cách học thuộc bảng tính tan là mục tiêu cơ bản để học môn hóa học. Kiến thức này rất cơ bản, nhưng cực kỳ quan trọng. Tuy nhiên, bảng tính tan của axit bazơ muối rất đa dạng, phong phú nên gây nhiều khó khăn cho ghi nhớ và vận dụng. Hôm nay, chúng tôi chia sẻ bảng tính tan mới nhất và đầy đủ nhất. Đồng thời, hướng dẫn các bạn cách học, cách ghi nhớ và vận dụng dễ dàng, hiệu quả nhất.
Bên cạnh bảng tuần hoàn hóa học thì bảng tính tan của Axit – Bazơ – Muối không kém phần quan trọng. Tính tan của các chất khác nhau, các kim loại với các gốc axit khác nhau. Nên tính tan gây khó nhớ cho người học, nên bảng tính tan sẽ giải quyết vướn mắt này nhé.
 Bảng tính tan đầy đủ nhất, mới nhất và đẹp nhất hiện nay
Bảng tính tan đầy đủ nhất, mới nhất và đẹp nhất hiện nay
1. Độ tan là gì?
Độ tan của một chất trong nước là số gam chất đó hòa tan trong 100g nước ở điều kiện nhiệt độ nhất định để tạo thành dung dịch bão hòa. Độ ta được kí hiệu là S.
Ví dụ: Ở nhiệt độ phòng (25 °C) giá trị độ tan của muối ăn (NaCl) là 36 g, độ tan của muối bạc nitrate (AgNO3) là 222 g, còn độ tan của đường là 204 g, …
2. Bảng tính tan là gì?
Bảng tính tan là bảng tổng hợp tính tan hay không tan của các chất trong nước. Tuy nhiên, tính tan của Axit – Bazơ – Muối rất đa dạng và phụ thuộc nhiều yếu tố.
Chất có thể tan hoàn toàn trong nước, chất khác ít tan hoặc thậm chí là không tan trong nước.
Bảng tính tan hóa học hay thường tổng hợp đầy đủ, dễ nhìn và biểu diễn trạng thái tan, ít tan và không tan của một chất ở 25,15 °C (293.15 K) và 1 atm.
3. Bảng tính tan của Axit – Bazơ – Muối
Đây là bảng tổng hợp tính tan của hầu hết các chất thường gặp trong hóa học phổ thông. Biết cách sử dụng và học cách ghi nhớ khoa học bảng tính tan sẽ giúp ít rất nhiều cho việc học tập hóa học. Hôm nay, chúng tôi tổng hợp kiến thức của bảng tính tan đầy đủ và mới nhất hiện nay. Bên cạnh đó, cách học thuộc bảng tính tan nhanh nhất sẽ giúp nằm lòng và vận dụng một cách nhanh chóng.
Tính tan của các chất phụ thuộc vào các yếu tố như nhiệt độ, áp suất,… nên tính tan rất khác nhau. Vì vậy, kiến thức tính tan của các chất trong bảng dưới đây, đơn giản, dễ nhận dạng và ghi nhớ tốt hơn.
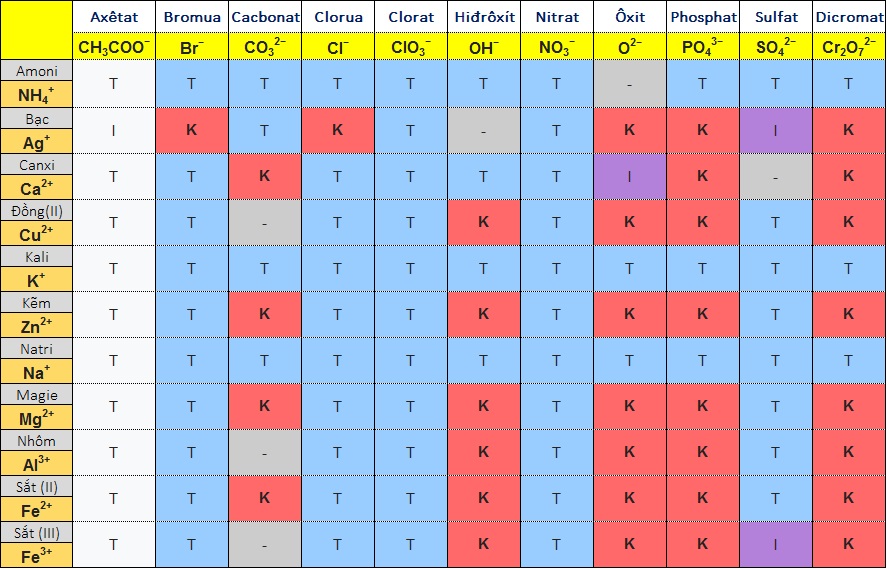
Bảng tính tan của axit bazơ muối đẹp nhất hiện nay
Các ký hiệu trong bảng tính tan:
– T: các hợp chất tan trong nước (không kết tủa).
– K: các hợp chất không tan trong nước (kết tủa.
– I: các hợp chất ít tan trong nước.
– Dấu “-“: Các hợp chất không tồn tại hoặc bị phân hủy.
Ngoài bảng tổng hợp tính tan của các chất, thì cách học làm sao cho hiệu quả. Sau đây, các bạn thử trải nghiệm cách học thuộc bảng tính tan nhanh và nhớ lâu nhất.
4. Cách học bảng tính tan nhanh nhất, dễ nhớ nhất
4.1. Tính tan của axit
– Tính chất hóa học chung của các axit là hòa tan tốt trong nước. Cho nên, đa số các axit tan tốt trong nước. Tuy nhiên, có một số axit không tan đó là: H2SO4, H3PO4 không bay hơi, H2SiO3, HNO3, HSO3 dễ phân hủy thành khí bay lên.
– Lưu ý axit yếu như H2CO3 , H2SO3 , là axit yếu (là axit có liên kết không bền) nên dễ dàng bị phân hủy trong nước, giải phóng khí CO2 , SO2 và nước.
4.2. Tính tan của bazơ
– Đặc tính cơ bản của kim loại là không tan trong nước. Tuy nhiên, bazo của các kim loại kiềm thì tan hoàn toàn trong nước. Các bazo của kim loại kiềm thổ ít tan tan trong nước.
– Hầu hết các kim loại tạo bazo tương ứng, nhưng AgOH và Hg(OH)2 không tồn tại.
4.3. Tính tan của muối
– Muối có gốc axit vẫn còn nguyên tử Hidro là muối axit. Các muối này hầu như tan tốt trong nước điển hình như (-HCO3, – HSO3, – HS).
– Muối của nhóm nitrat, muối Axetat tan tốt trong nước
– Muối Photphat (-PO4)3- của các kim loại kiềm thì tan, còn lại thì không tan.
– Muối gốc Cacbonat (- CO32-) hầu như không tan, ngoại trừ muối của các kim loại kiềm. Các kim loại Hg, Al, Cu, Fe (III) tạo không tồn tại muốn với gốc cacbonat hoặc bị phân hủy trong nước.
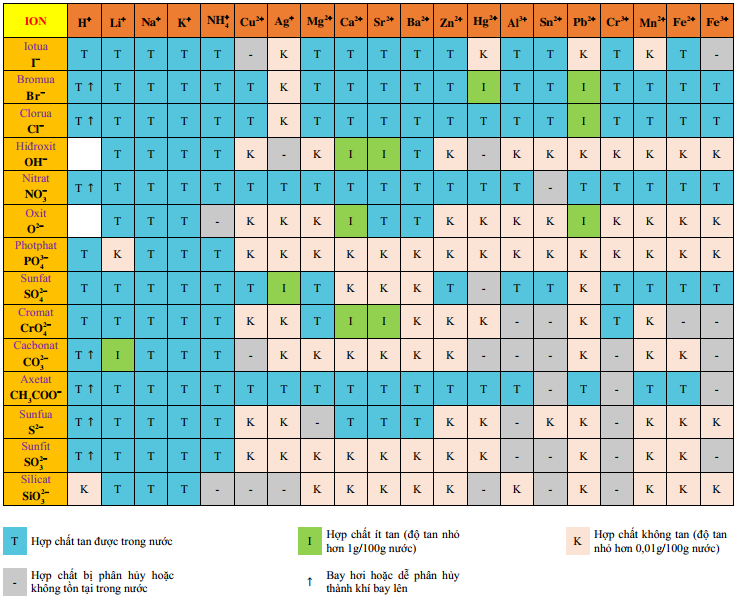 Môt dạng khác của bảng tính tan đầy đủ, nhiều hợp chất hơn
Môt dạng khác của bảng tính tan đầy đủ, nhiều hợp chất hơn
– Muối chứa lưu huỳnh có nhiều gốc axit cần phải nhớ. Đó là nhóm Sulfua (-S), Sulfit (-SO32-) và Sulfat (-SO42-). Tất cả các muối của lưu huỳnh với kim loại kiềm và kiềm thổ đều tan trong nước. Nhưng đối với các kim loại khác thì muối sunfua và sulfate khóa tan, không tồn tại MgS và Al2S3 và muối Sulfit của Al và Fe (III). Muối Sulfat thường gặp nhất, muối này dễ tan. Ngoại trừ BaSO4, PbSO4, SrSO4 không tan. CaSO4, Ag2SO4 ít tan và HgSO4 không tồn tại.
– Muối Silicat (-SiO3) rất khó tan trong nước. Tuy nhiên, trừ muối của đứng đầu trong bảng tuần hoàn hóa học (kim loại kiềm và kim loại kiềm thổ) như Na2SiO3, K2SiO3… thì tan. Muối Siliacat của Hg, Cu, Ag thì không tồn tại.
– Muối của các halogen: -F, -Cl, -Br, -I gần như tan. Ngoại trừ các muối kết tủa không tan như AgCl, AgBr, AgI không tan. 3 loại muối này gặp phổ biến nhất trong các bài tập, đặc biệt là bài toán nhận biết hóa chất. Muối của kim loại chì với Clo là PbCl2 ít tan và không tồn tại muối AgF.
– Đứng thứ 2 sau muối của Sulfat (-SO42-) là muối cacbonat (-CO32-) hầu như không tan được. Tuy nhiên, của hidrocaconat thì tan trong nước như NaHCO3, Ca(HCO3)2 … Ngoài ra, muối các kim loại kiềm, kiềm thổ như Na, Li, K,…tan được trong nước.
Bảng tính tan đầy đủ nhất được trình bày đẹp mắc, dễ nhìn hơn. Ngoài kiến thức tính tan của các nguyên tố hóa học thì chúng tôi chia sẽ cách học bảng tính tan nhanh, nhớ lâu. Các học này, giúp các bạn cũng cố kiến thức vững chắc và lâu dài. Giúp vận dụng các tính tan để giải thích hiện tượng trong phản ứng, phân tích tính chất của các chất,… Thực ra, mỗi người có cách học khác nhau dựa vào đặc điểm của của bảng tính tan. Chúc các bạn học tốt và thường xuyên cạp nhật thêm các kiến thức hóa học tại Từ Điển Hóa Học nhé!















hay